Metalle im Smartphone von Richard & Nick
Eigenschaften, Verwendung und ökologischer Fußabdruck
1. Übersicht: Metalle im Smartphone
Ein Smartphone enthält über 30 verschiedene Metalle. Jedes Metall erfüllt seine eigne Funktion da sie alle spezifische Eigneschafften haben.
| Komponente | Verwendete Metalle | Hauptfunktion des Metalles |
|---|---|---|
| Touchscreen | Indium (In), Silizium (Si), Zinn (Sn) | Transparente, leitfähige Schicht |
| Leiterplatte | Gold (Au), Silber (Ag), Kupfer (Cu), Palladium (Pd) | Elektrische Verbindungen |
| Akku | Lithium (Li), Kobalt (Co), Nickel (Ni), Mangan (Mn) | Energiespeicherung |
| Gehäuse | Aluminium (Al), Magnesium (Mg) | Stabilität bei geringem Gewicht |
| Kamera-Magnete | Neodym (Nd), Dysprosium (Dy), Eisen (Fe) | Autofokus, Bildstabilisierung |
| Vibrationsmotor | Wolfram (W), Dysprosium (Dy) | Haptisches Feedback |
2. Metalle und ihre eigenschafften
Kupfer (Cu) - Leiterbahnen
Genutzte Eigenschaft: Sehr hohe elektrische Leitfähigkeit
Warum ist es geeignet? Kupfer leitet elektrischen Strom nahezu verlustfrei und ist kostengünstiger als Silber. Es ermöglicht schnelle Signalübertragung bei minimalen Energieverlusten in allen Leiterbahnen der Hauptplatine.
 Quelle
Metallgitter
Quelle
Metallgitter
Gold (Au) - Kontakte und Verbindungen
Genutzte Eigenschaft: Rostbeständig & gute Leitfähigkeit
Warum geeignet? Gold oxidiert nicht und behält seine Leitfähigkeit dauerhaft bei. Kritische Kontakte (Prozessor, SIM-Karte, Steckverbindungen) bleiben zuverlässig, auch nach Jahren der Nutzung. Keine Oxidschicht blockiert den Stromfluss.
 Quelle
Metallgitter
Quelle
Metallgitter
Lithium (Li) - Akku
Genutzte Eigenschaft: Höchste Energiedichte aller Metalle (260 Wh/kg)
Warum geeignet? Lithium kann sehr viel Energie pro Gewichtseinheit speichern. Es ist das leichteste Metall und hat ein sehr negatives Standardpotential (-3,04 V), was hohe Spannungen ermöglicht. Der Akku bleibt kompakt und leicht.

 Quelle
Quelle
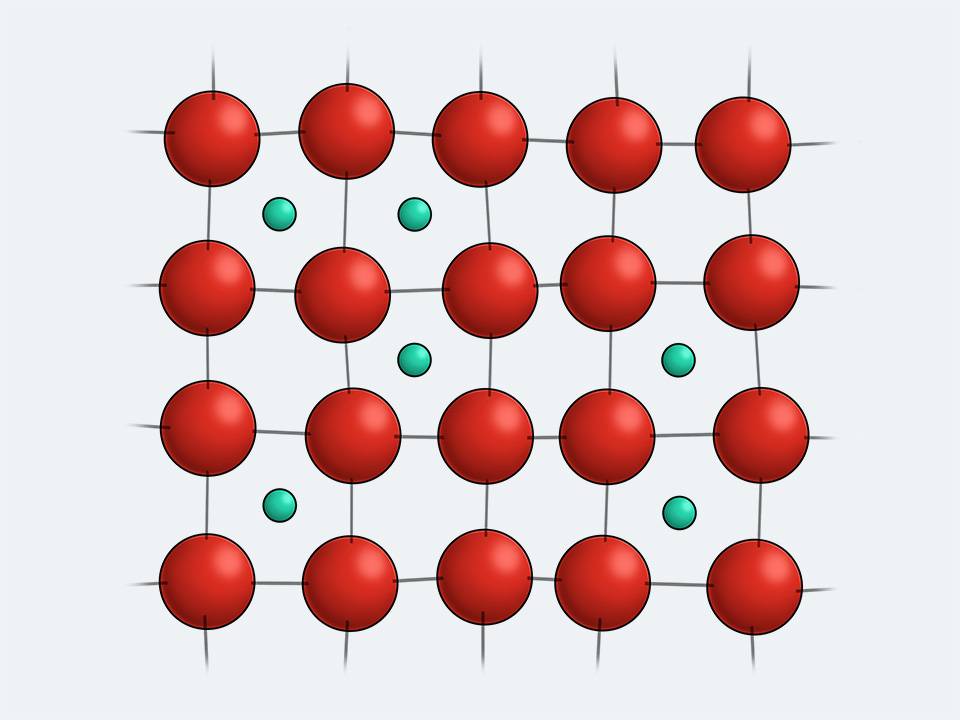
Neodym (Nd) - Magnete
Genutzte Eigenschaft: Stärkste permanentmagnetische Eigenschaften
Warum geeignet? Neodym-Magnete (NdFeB) erzeugen extrem starke Magnetfelder bei kleinster Größe. Sie sind bis zu 10-mal stärker als herkömmliche Magnete und ermöglichen präzise Autofokus-Bewegungen und kraftvolle Lautsprecher.

 Quelle
Quelle
Indium (In) - Touchscreen
Genutzte Eigenschaft: Transparent + elektrisch leitfähig
Warum geeignet? Indium-Zinn-Oxid (ITO) ist eines der wenigen Materialien, das gleichzeitig durchsichtig und leitfähig ist. Die transparente Leiterschicht auf dem Display erfasst Berührungen, ohne das Bild zu blockieren.

 Quelle
Quelle
Aluminium (Al) - Gehäuse
Genutzte Eigenschaft: Geringes Gewicht + hohe Festigkeit + gute Wärmeableitung
Warum geeignet? Aluminium hat nur ein Drittel der Dichte von Stahl, ist aber sehr fest. Es leitet Wärme gut ab (schützt Prozessor vor Überhitzung) und lässt sich präzise bearbeiten.
 Metallgitter
Quelle
Metallgitter
Quelle
3. Struktur-Eigenschaften und deren Beziehung
Kernfrage: Warum haben diese Metalle die beschriebenen Eigenschaften?
Sie können die eingebettete Seite über den folgenden Verweis aufrufen: SELFHTML
Grundprinzip: Metallische Bindung
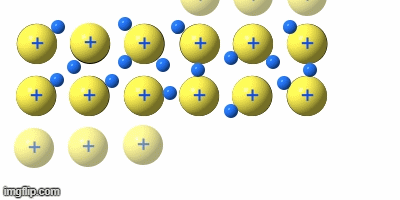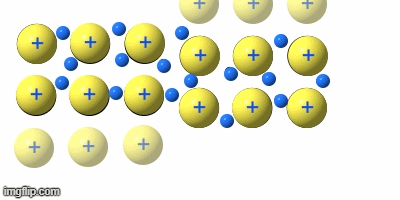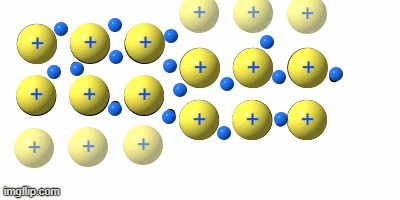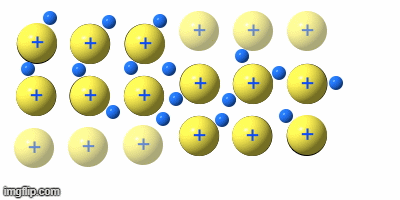
Die Grundstruktur aller Metalle ist identisch: Ein Gitter aus positiv geladenen Atomkernen wird von einem „Meer“ frei beweglicher Elektronen (Elektronengas) umgeben. Die Valenzelektronen sind nicht an bestimmte Atome gebunden.
Formel: Metallatome → Metallkationen + Elektronengas
Elektrische Leitfähigkeit (Kupfer)
Struktur: Frei bewegliche Valenzelektronen im Metallgitter
Warum leitfähig? Diese Elektronen können sich unter elektrischer Spannung gerichtet bewegen = elektrischer Strom. Kupfer-Atome geben ihr äußerstes Elektron ab, diese bewegen sich frei und transportieren Ladung schnell.
Warum ist Kupfer besser, als andere Metalle wie Eisen? Kupfer hat eine dichtere Elektronenwolke mit höherer Beweglichkeit, weniger Streuung an Kristalldefekten.
Korrosionsbeständigkeit (Gold)
Struktur: Sehr hohe Elektronegativität und geschlossene Elektronenschalen
Warum korrosionsbeständig? Gold reagiert nicht mit Sauerstoff, weil die Oxidation energetisch ungünstig ist. Die äußeren Elektronen sind stark an den Kern gebunden (relativistische Effekte). Gold bleibt dauerhaft metallisch und leitfähig da es ein Edelmetall ist.
Magnetismus (Neodym, Eisen)
Struktur:Ungepaarte Elektronen in den d- und f-Orbitalen
Warum magnetisch? Diese ungepaarten Elektronen weisen magnetische Momente (Spin) auf. Neodym, ein Seltenerdmetall, weist viele ungepaarte f-Elektronen auf. Zusammen mit Eisen und Bor bilden sie NdFeB-Magnete, deren magnetische Momente extrem stark und parallel ausgerichtet sind.
Ferromagnetismus:Atome in der Nachbarschaft koppeln ihre Spins parallel → makroskopisches Magnetfeld
Hohe Energiedichte (Lithium)
Struktur: Kleinstes und leichtestes Metall (Ordnungszahl 3, Atommasse 6,94 g/mol)
Warum so energiereich? Lithium gibt sein einziges Valenzelektron sehr leicht ab. Sehr niedriges Standardpotential (-3,04 V). Pro Gewichtseinheit können sehr viele Li⁺-Ionen Ladung transportieren.
Im Akku: Lithium-Ionen (Li⁺) bewegen sich zwischen der Anode (Graphit) und der Kathode (Metalloxid). Da Lithium ein geringes Gewicht hat, kann der Akku eine große Energiemenge speichern.
Transparenz + Leitfähigkeit (Indium-Zinn-Oxid)
Struktur:Indiumoxid (In₂O₃), dem ein gewisser Anteil von Zinn (Sn) zugesetzt wurde.
Warum transparent? Durchsichtig für sichtbares Licht, aber nicht für UV-Licht.
Warum leitfähig? Das Zinn, das wir hinzufügen, liefert freie Elektronen. Dadurch leitet das ITO Elektrizität, bleibt aber trotzdem durchsichtig.
Geringes Gewicht + Festigkeit (Aluminium)
Struktur: Würfelförmige Gitterstruktur mit relativ geringer Dichte (2,7 g/cm³).
Warum leicht und fest? Leichte Atome sind ziemlich dicht beieinander; das Material bleibt stabil und ist trotzdem noch leicht.
Oxidschicht: Aluminium bildet von selbst eine dünne Oxidschicht (Al₂O₃), die es vor weiterer Korrosion schützt.
Wärmeableitung: Viele freie Elektronen transportieren nicht nur Strom, sondern auch Wärme effizient.
4. Ökologischer Fußabdruck
Wichtige Fakten:
Die Herstellung eines einzigen Smartphones braucht:
- Ca. 13 Tonnen Wasser
- Ca. 18 m² Land
- Verursacht ca. 85 kg CO₂ Emissionen
Der Großteil der Umweltbelastung entsteht beim Abbau und der Verarbeitung der Metalle. Hohe Umweltbelastung bedeutet, dass unsere Umwelt stark verschmutzt oder geschädigt wird, zum Beispiel durch Abgase, Müll oder Chemikalien. Dazu gehören viele Autos mit Abgasen, Fabriken mit Rauch und Chemikalien sowie viel Plastik und Müll in der Natur.
Kritische Metalle & Hohe Umweltbelastung
Kobalt (Co) - Akku
Abbau: Hauptsächlich in Kongo (70% der Weltproduktion)
Ressourcenverbrauch:
- Hoher Wasserverbrauch: ca. 400.000 Liter für eine Tonne Kobalt
- CO₂ Emissionen: 6 Tonnen CO₂ pro Tonne Kobalt
Umweltbelastung:
- Das Grundwasser wird durch Schwermetalle verunreinigt werden.
- Zerstörung von Landschaften durch Tagebau
- Oft in Minen mit schlechten Arbeitsbedingungen und teilweise Kinderarbeit
Transport: Weite Transportwege aus Afrika nach Asien zur Weiterverarbeitung und zu der Kundschaft
Neodym (Nd) & Seltene Erden für Magnete
Abbau: Hauptsächlich China (80% der Produktion)
Ressourcenverbrauch:
- Pro Tonne Neodym: Beim Abbau von Neodym fallen rund 2.000 Tonnen nutzloses Gestein und Chemikalienabfälle an.
- Gewinnung ist schwierig und braucht viel Energie.
Umweltbelastung:
- Radioaktive Abfälle durch Thorium und Uran im Erz
- Große Luftverschmutzung durch Säuredämpfe
- Zerstörung großer Landflächen durch Tagebau
- Verunreinigung von Gewässern mit Säuren und radioaktiven Stoffen
Gold (Au) - Kontakte
Abbau: Südafrika, China, Australien, Russland
Ressourcenverbrauch:
- Extrem ressourcenintensiv: Für 1g Gold werden 2-3 Tonnen Gestein bewegt
- CO₂ Emissionen: 16 Tonnen CO₂ pro Kilogramm Gold
- Für ein Smartphone (0,024g Gold): ca. 70-80 kg Gestein
Umweltbelastung:
- Einsatz von hochgiftigem Cyanid (hochtoxische Salze und Verbindungen der Blausäure) zur Goldgewinnung
- Verschmutzung von Flüssen und Grundwasser mit Quecksilber und Zyanid
- Massive Zerstörung von Landschaften durch Tagebau
Indium (In) - Touchscreen
Abbau: Nebenprodukt von Zink und Bleigewinnung
Ressourcenverbrauch:
- Begrenzte Verfügbarkeit Ressourcen könnte in 20-30 Jahren erschöpft sein
- Die Reinigung braucht sehr viel Energie.
- Preis stark gestiegen aufgrund hoher Nachfrage
Mittlere Umweltbelastung
Kupfer (Cu) Leiterbahnen
Abbau: Chile, Peru, China, USA
Ressourcenverbrauch:
- Hoher Energiebedarf: ca. 3-4 Tonnen CO₂ pro Tonne Kupfer
Umweltbelastung:
- Großflächiger Tagebau mit Landschaftszerstörung
- Beim Schmelzen entsteht Schwefeldioxid, das die Luft verschmutzt.
Positiv: Gut recycelbar ohne Qualitätsverlust
Lithium (Li) - Akku
Abbau: Australien (Festgestein), Chile/Argentinien (Salzseen)
Ressourcenverbrauch:
- Extrem hoher Wasserverbrauch: 2 Millionen Liter pro Tonne Lithium in Südamerika
- CO₂ Emissionen: 5 Tonnen pro Tonne Lithium
Umweltbelastung:
- Grundwasserspiegel in Atacama stark gesunken
- Bedrohung indigener Lebensräume und lokaler Ökosysteme
- Verschmutzung von Salzseen
Vergleichsweise geringe Belastung
Aluminium (Al) Gehäuse
Abbau: Bauxit-Abbau in Australien, China, Guinea
Ressourcenverbrauch:
- Sehr energieintensiv bei Erstherstellung: 10-15 Tonnen CO₂ pro Tonne Aluminium
- Hoher Stromverbrauch bei der Elektrolyse (ca. 15.000 kWh pro Tonne)
Umweltbelastung:
- Tagebau führt zu Landschaftsveränderungen
- "Rotschlamm" als giftiges Abfallprodukt
Positiv: Recycling spart 95% der Energie gegenüber Neuproduktion. Sehr gut und oft recycelbar.
Fazit und Lösungsansätze
Hauptprobleme:
- Hoher Ressourcenverbrauch (Wasser, Energie, Land)
- Massive Umweltverschmutzung (Gewässer, Luft, Boden)
- Soziale Probleme (Arbeitsbedingungen, Kinderarbeit)
- Lange Transportwege erhöhen CO₂-Ausstoß
Lösungsansätze:
- Recycling: Aus 1 Tonne alter Handys kann man mehr Gold gewinnen als aus 1 Tonne Golderz
- Längere Nutzung: Smartphones länger nutzen reduziert Gesamtbelastung
- Faire Rohstoffe: Zertifizierung und faire Abbaubedingungen
- Materialsubstitution: Forschung an Alternativen (z.B. Natrium statt Lithium)
- Reparatur statt Neukauf: Modulare Bauweise ermöglicht Reparaturen
Lerning apps:
Rechtliche Hinweise
Impressum
Betreiber: Richard & Nick
Haftung: Trotz sorgfältiger inhaltlicher Kontrolle übernehmen wir keine Haftung für Inhalte externer Links.
Datenschutzerklärung
Diese Website erhebt keine personenbezogenen Daten direkt. Beim Einbinden von Videos über LearningApps.org werden jedoch Daten an die Drittanbieter übertragen. Weitere Informationen finden Sie unter: https://learningapps.org/datenschutz.
Haftungsausschluss
Die Inhalte dieser Website dienen ausschließlich Bildungszwecken. Wir übernehmen keine Gewähr für die Aktualität, Richtigkeit oder Vollständigkeit der Informationen. Für Schäden, die durch die Nutzung der Inhalte entstehen, wird keine Haftung übernommen.
Urheberrecht
Alle Texte, Grafiken und Bilder auf dieser Website sind urheberrechtlich geschützt. Inhalte, die von Dritten stammen, werden als solche gekennzeichnet und verlinkt. Die Verwendung ohne Genehmigung ist nicht gestattet.